Немного физики
Для начала небольшое пояснение для тех, кто физикой никогда особо не интересовался. Я не буду использовать формулы и сложные термины, а всю теорию буду безбожно упрощать. Если же вы хорошо знаете термодинамику, то лучше пропустите этот раздел во избежание приступов праведного гнева. Итак, начнем.

Как вы помните, XIX век стал веком пара. По рельсам бегали паровозы, по морям плавали пароходы, а на заводах массово устанавливали различные паровые машины. Естественно, что перед инженерами и учеными была поставлена задача — выжать максимум из всей этой техники. И для решения этой задачи появился новый раздел физики — термодинамика.
Первоначально она в основном изучала превращение энергии пара в механическую работу. Но со временем термодинамика вышла за пределы паровых котлов и стала заниматься вообще всеми системами, которые состоят из большого числа каких-нибудь частиц (например, молекул).
А к таким системам относится почти все, что мы с вами видим вокруг себя. Это и накачанный воздухом мяч, и бутылка с водой, и письменный стол, и наша планета, и даже вся вселенная.

У термодинамики есть несколько законов, которые обычно называют началами. Первое начало — это, по сути, всем знакомый закон сохранения энергии, но с поправкой на особенности термодинамических систем.
А вот второе начало более необычное. Оно было открыто еще в XIX веке, когда в центре внимания термодинамики в основном находились так называемые тепловые машины. К таковым относятся все механизмы, которые умеют превращать тепло в механическую энергию: паровая машина, современный двигатель внутреннего сгорания и даже реактивный двигатель.
Выяснилось, что заставить тепловую машину работать можно лишь тогда, когда в ней есть хоть какая-нибудь разница температур. То есть в любой из таких машин должны присутствовать источник тепла с высокой температурой и источник с низкой температурой. Если же у нас есть только один источник тепла, то как бы сильно мы его ни нагревали, мы ничего от нашей машины не добьемся.
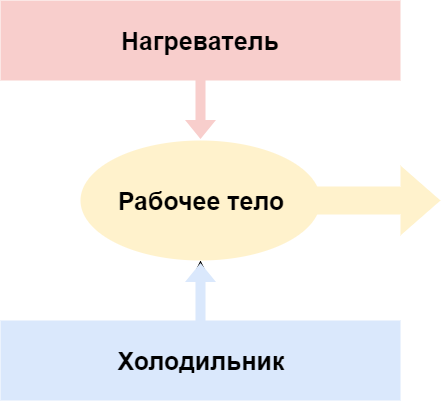
Из этого наблюдения ученые и вывели второе начало термодинамики. В настоящее время у него существуют десятки формулировок. Вот, например, одна из них:
Никакое устройство не может извлечь работу из системы, которая вся целиком находится на одном потенциальном уровне.
Если же у нас есть два разных энергетических уровня, то система придет в движение. Например, тепло потечет от горячего тела к холодному, а электрический ток побежит от анода к катоду. И чем больше эта разница между потенциалами, тем больше полезной работы может совершить система.
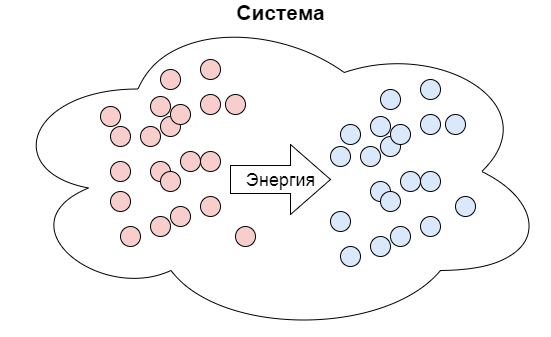
Поэтому второе начало можно сформулировать еще вот так:
Поток энергии в системе всегда направлен от высокого потенциала к низкому.
Теперь представим, что мы каким-то образом изолировали систему от внешнего мира, и в нее больше не проникают ни вещество, ни энергия. Что произойдет в этом случае?
А в этом случае разность между потенциалами будет постепенно уменьшаться. Горячее тело со временем остынет, а холодное — нагреется. И это значит, что будет уменьшаться и количество энергии, которую мы могли бы превратить в полезную работу.
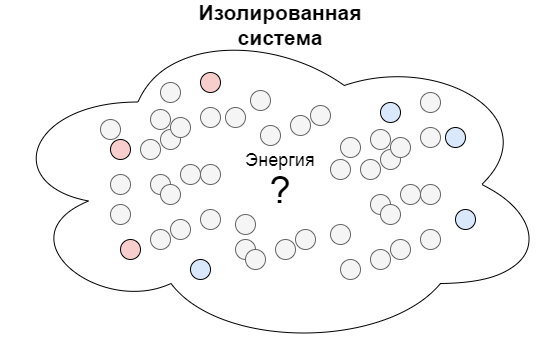
Чтобы измерить эту безвозвратно потерянную полезную энергию, ученые придумали специальную величину — энтропию. Чем больше энергии было безвозвратно потеряно, тем выше в системе энтропия. Из этого следует еще одна формулировка второго начала:
В любой изолированной системе полная энергия остается постоянной, а полная энтропия с течением времени возрастает.
Или более строго:
В изолированной системе энтропия остается либо неизменной, либо возрастает в неравновесных процессах.
А теперь обратите внимание: в самом начале в нашей системе наблюдался какой-то элементарный порядок, например, деление на горячую и холодную часть. Но после увеличения энтропии, система стала приходить в беспорядочное, хаотичное состояние. И как доказал австрийский физик Больцман, энтропия — это и есть мера неупорядоченности системы.
На самом деле энтропия понятие сложное, поэтому для его объяснения часто прибегают ко всяким метафорам. Например:

К сожалению, метафоры не совсем точно отражают реальность. Например, осколки льда выглядят более хаотично, чем графин с водой. Но в действительности у жидкой воды энтропия значительно выше.
Итак, надеюсь, что со вторым началом термодинамики мы разобрались. Еще раз: в любой изолированной системе энтропия со временем возрастает или, в идеальном случае, остается неизменной.
Креационизм и второе начало
Второе начало термодинамики оказало огромное влияние не только на физику, но и на философию. Именно из него выросли такие понятия, как «демон Максвелла», «вечный двигатель второго рода» и «тепловая смерть вселенной».
Как ни странно, но популярно второе начало и у креационистов. Они регулярно поминают его в своих проповедях и посвящают ему обширные статьи. А все потому, что в нем креационисты видят один из главных доводов против теории эволюции.
Вот как выглядят типичные их рассуждения:
Ваша эволюция — это самопроизвольное упорядочивание материи. Во время эволюционных процессов неживые молекулы (нуклеотиды и аминокислоты) якобы сами собой образуют живые и упорядоченные системы. И эти системы не просто существуют: они порождают себе подобных и даже развиваются в сторону большего порядка.
Но согласно второму закону термодинамики, все системы стремятся к увеличению энтропии и возрастанию хаоса, а не к порядку! Если мы, например, оставим без присмотра свою «Ладу Калину», то со временем она заржавеет и развалится, а не превратиться в сверкающий лимузин.
И это значит, что второй закон термодинамики фактически запрещает любую самоорганизацию материи. Более того, без вмешательства извне вообще невозможна никакая жизнь! Ведь энтропия (от которой за версту несет чем-то инфернальным) рано или поздно ее уничтожит.
Эволюционисты не знают, как объяснить это противоречие. А потому вся теория эволюции существует исключительно в их фантазии.
Что из этого следует? Правильно: приходите к нам на собрание в следующее воскресенье.
А как на самом деле?
Оставим за скобками вопрос, насколько применимо понятие энтропии к эволюции. И не будем обращать внимание на весьма вольную трактовку креационистами второго начала. Перейдем непосредственно к их главной претензии.
Как вы помните, сперва термодинамика занималась изучением тепловых машин. А поэтому давайте и мы для начала внимательно посмотрим на эти машины.
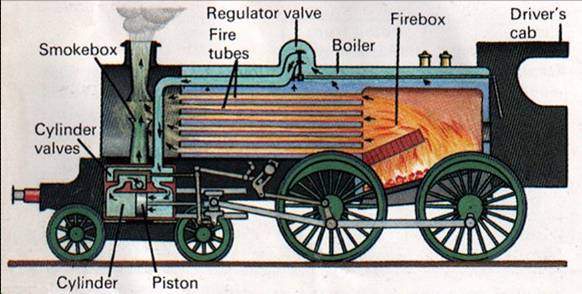
На чем основана их работа? Если отбросить технические детали, то она сводится к преобразованию хаотично движущихся частиц в упорядоченное движение колес или рычагов. Нарушает ли это второе начало термодинамики?
Нет, не нарушает. Машины работают за счет разрушения химических связей топлива, а это приводит материю в состояние еще более высокой энтропии. Тем более что машина превращает в механическую работу только часть энергии топлива, а остальная рассеивается в виде бесполезного тепла.
Тут кто-нибудь может возразить:
— Но ведь это механизмы, созданные человеком!
Но тепловые машины, которые преобразуют хаос в упорядоченное движение, есть и в природе. К ним относятся морские течения, циклоны, муссоны, пассаты, тайфуны и многое другое. А одним из самых впечатляющих примеров природных тепловых машин считаются ячейки Бенара. Вот, например, результат их работы:

Точно такими же тепловыми машинами являются и все живые организмы. Это и отдельные органеллы (например, рибосомы и митохондрии), и целые клетки, и многоклеточные организмы, и даже экосистемы.
Им всем, как и обычным машинам, для работы необходимо свое топливо. Растениям для нормального роста нужна солнечная энергия и минеральные вещества из почвы. Корова, чтобы совершать свою «полезную работу», должна есть траву, а волку для этого нужно есть зайцев.
Более того: такой тепловой машиной является вся биосфера Земли. Она потребляет солнечную энергию и утилизирует излишки тепла в космическое пространство.
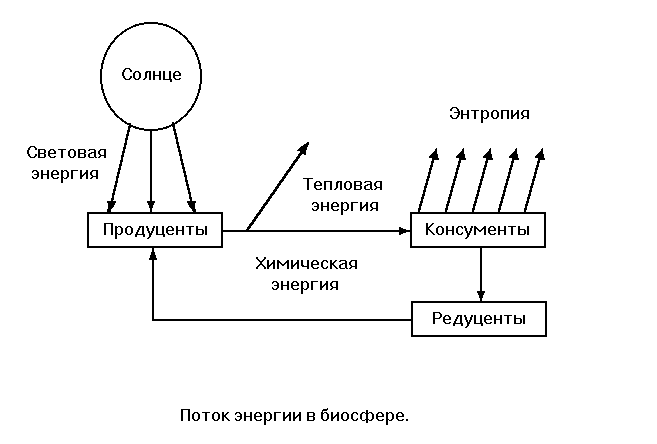
Ошибка креационистов в том, что второе начало термодинамики применимо только к изолированным системам, которые не обмениваются с внешней средой ни веществом, ни энергией.
Однако ни Земля, ни биосфера, и ни одно живое существо не изолированы от окружающей среды. Они не существуют сами по себе: они постоянно потребляют внешнюю энергию, а потому являются открытыми системами.
Что же касается энтропии, то все «живые тепловые машины» уменьшают ее лишь в одной точке пространства и лишь на короткое время. При этом уменьшается она всегда за счет внешней среды, где энтропия из-за этого возрастает.
Заключение
На самом деле описание жизни и эволюции в категориях термодинамики — тема действительно очень интересная. Однако она гораздо сложнее, чем это пытаются представить креационисты и отнюдь не сводится к поверхностным суждениям. Сегодня термодинамика биологических процессов является одним из перспективных направлений биофизики, которая изучает физические аспекты жизни во всех ее проявлениях.
Сама же неравновесная термодинамика, в сферу которой как раз попадают жизнь и эволюционные процессы, сформировалась только в XX веке. В наше время она активно развивается, и вполне возможно, что впереди нас ждут новые открытия в области эволюционной теории.


